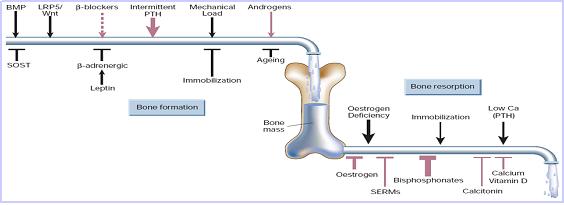
Determinants of skeletal homeostasis and bone mass
osteoblast (그리스 어원 : bone + germ)는 세포 밖으로 골질을 분비하고 스스로는 골질에 싸여 골세포로 변함으로써 bone formation을 담당한다. 이것은 섬유모세포에서 분화하여 분열능력이 크며 cbfa1/RUNX2와 Wnt signal pathway에 의해 조절된다. 또한osteoblast는 osteoclast 분화인자인 RANKL을 발현시킴으로써 osteoclast의 분화에도 관여 한다. 반면 osteoclast(그리스 어원 : bone + broken)는 주로 bone resorption을 담당하며
osteoclast 로의 분화는 macrophage colony stimulating factor(M-CSF), Receptor for Activation of Nuclear Kappa B Ligand(RANKL), osteoprotegerin(OPG)에 의해 조절된다. 이것은 끊임없는 파괴과정의 매개자로서 osteoblast와 상반된 작용을 하기 때문에 osteoporosis / RA 치료의 target cell이 될 수 있고, osteoblast와 osteoclast사이의 balance는 bone formation 및 bone mass 의 Key factor라 할 수 있다.
Rheumatoid arthritis(류마티스 관절염)
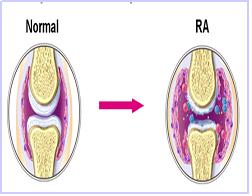
bone strength 및 integrity은 osteoblast / osteoclast / synoviocyte 사이의 섬세한 balance에 의존하여 유지되며 이러한 balance에 문제가 생겼을 때 뼈 질환이 야기된다. 특히 Rheumatoid Arthritis는 이물질에 대한 체내 면역체계에 이상이 생겨 이물질을 공격해야 할 면역세포가 오히려 관절을 싸고 있는 얇은 윤활막(Synovial membrane)을 공격하여 발생하는 자가 면역 질환이다. 이는 주로 말초 관절에서 대칭적인 형태로 염증이 생성되며 전신성ㆍ난치성ㆍ만성 염증질환으로 분류 할 수 있다.
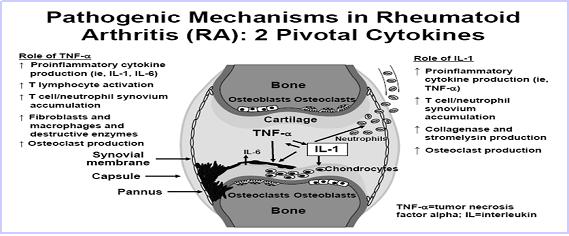
Rheumatoid arthritis(류마티스 관절염) 분자기전
RANKL 과 RANK
RANKL과 RANK는 각각 TNF(Tumor Necrosis Factor)의 member와 TNF receptor superfamily이다. osteoclast와 osteoclast의 전구체에 있어서 RANK의 존재는 Stromal cell에 존재하는 osteoclast 분화의 key factor가 RANKL일 것이라는 증거가 된다. 이와 함께 활성화된 T lymphocyte는 inflammatory cytokine을 분비(IL-1β,IL-17,IL-23)하여 synoviocyte(활막세포)를 증식시킴으로서 RANKL을 과발현 시켜 직접적으로 osteoclastogenesis(macrophage activation)을 촉진시킨다. 즉 , RANKL은 osteoclast분화에 있어서 Stromal cell/osteoblast에 의해 중요한 역할을 담당한다. 그리고 stromal cell/ osteoblast는 대부분의 osteoclastogenic agent 의 target이며 osteoclastogenic agent는 RANKL발현을 강화시켜 효과를 발휘한다.
Osteoclastogenic cytokine
RA는 관절의 연골조직의 파괴에 의해 혹은 연골아래의 과도한 osteoclastic bone resoption에 의해 유발되는데 염증상태에서는 osteoclast로 분화될 macrophage가 Rheumatoid synovial membrane에 축적되며, 이곳에는 다양한 osteoclastogenic cytokine 이 존재한다.
e. g. IL-1,6,11,13
Rheumatoid synovial fibroblast는 RANKL을 생성하게 되는데 RANKL을 생성하는 T cell은 다른 cell의 참여 없이 osteoclast 형성을 촉진시킬 수 있다. Rheumatoid joint 또한 osteoclast형성의 inhibitor로 알려져 있다.
e. g. IL-18
이것은 M-CSF(granulocyte macrophage-colony stimulating factor)의 생산을 증가시키는 T cell에서 작동하는 것에 의해 osteoclast의 형성을 저해하며 rheumatoid synovium에서 pro-inflammatory effect를 가진다. 또 다른 osteoclast inhibitor로는 IFN-Γ, IL-12등이 있다.
e. g. IL-17
활성화된 CD+4 T림프구에서 생성되며 RA 환자의 혈청 및 관절에서 증가되며 RA 동물모델인 collagen-induced arthritis (CIA)에서 관절염 발생 초기 및 발생 후기에 관절염증의 악화와 골 파괴를 일으키는 주요한 역할을 하여 IL-17의 기능을 억제하여 RA을 치료하는 치료전략의 목표로 인식되는 주요한 사이토카인이다.
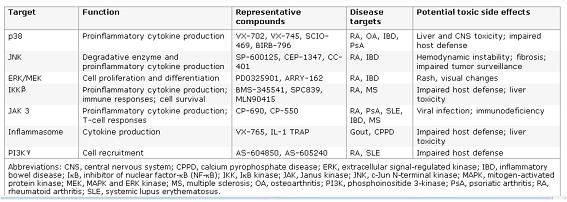
Rheumatoid arthritis(류마티스 관절염)의 치료
- Potential intracellular targets for biologic therapy of RA
관절에 존재하는 미성숙한 osteoclast가 분화하면서 IP-10이 생성되고 이 단백질이 CD4 T세포에 영향을 미쳐 TNF-α(Tumor Necrosis Factor)와 RANKL의 생성을 촉진함으로써 관절염의 골 흡수를 촉진시킨다. 실제로 IP-10에 대한 항체치료를 함으로써 관절염이 어느 정도 예방이 되는 것을 볼때, IP-10이라는 면역단백질이 관절염 치료제 개발의 새로운 중요 target이 된다고 설명 할 수 있다. 이처럼 본 실험실에서는 다양한 cyrokine과 TNF-α를 target으로 한 면역계의 조절을 통한 치료제 개발의 긍정적인 평가를 기대하고 있다.
현 과학기술의 발달과 생활환경 개선에 따른 건강한 노후에 대한 욕망의 일반화는 뼈질환을 연구하는 bone biology의 중요성을 강조한다. 이와 마찬가지로 본 실험실에서는 류마티스성 질환의 자가 면역 기전을 체계적으로 규명하고자 노력하고 있다. 이러한 시도는 이 질환군에 대한 이해를 높일 수 있을 뿐만 아니라 조기 진단, 면역 역학적 분류 예후의 예측 및 새로운 치료법 개발 등에 대한 기본적인 자료를 제공한다는 점에서 대단히 중요하다.
 분자의생명과학연구실
분자의생명과학연구실